
在唐朝的長安城,被剪刀劃傷手指的裁縫會把長著「綠毛」的漿糊抹在傷口上幫助愈合。這是歷史記載的最早的抗生素。
一千多年後地球另一邊,英國細菌學家在葡萄球菌的培育中偶然發現了圍繞在青黴素週邊的無菌圈,至此科學家的註意力才開始轉移到提取青黴素的方法上。但青黴素大量的應用於傷口救治還要等到二戰期間。
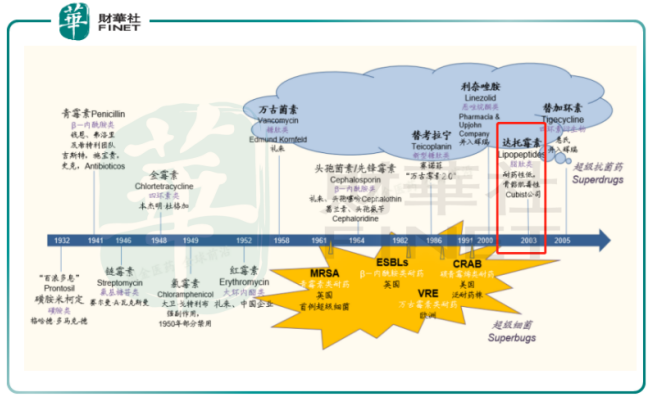
早期的青黴素殺菌機理簡單。它通過抑制細菌細胞壁形成的方式阻斷細菌繁殖,但人類不科學的濫用,令致病菌產生俞強的耐藥性。從1941年的青黴素,到2005年的替加環素,短短數十年已有11種抗生素面世,來抵抗不斷進化的細菌。
20世紀至今,人類的抗生素研發史徹底演變成一部超級細菌(superbugs)vs超級抗菌藥(superdrugs)的抗爭史。被譽為「耐藥菌最後一道防線」的萬古黴素(1952年,禮來)漸失其效(vs革蘭氏陽性耐藥菌),其「後繼者」達託黴素的上市,開啓了抗生素領域的新紀元。
上市初期的達託黴素,受限於抗生素口服的用藥習慣、較高的用藥成本和較弱的推廣力度,市場認可度低。2017年,國内達託黴素市場由Cubist(41.64%)、海正藥業(600267-CN)(33.06%)、恒瑞醫藥(600276-CN)(15.41%)和華東醫藥(000963-CN)(9.90%)主領(來源PDB),其中海正、恒瑞、華東生產的是原研藥「克必信」的仿製藥。

12月31日,研發超級抗菌藥的平台盟科醫藥-B申請赴港上市。招股書顯示,這家醫藥研發平台的優勢在於其預計最快實現商業化的MRX-1與達託黴素是治療同適應症的抗生素。與達託黴素相比,MRX-1將憑何斬獲市場?叠代甚於腫瘤的抗生素領域,盟科醫藥的研發能夠跟得上步伐?它又要靠什麽來突破當前的競爭格局?
超級抗菌藥MRX-1
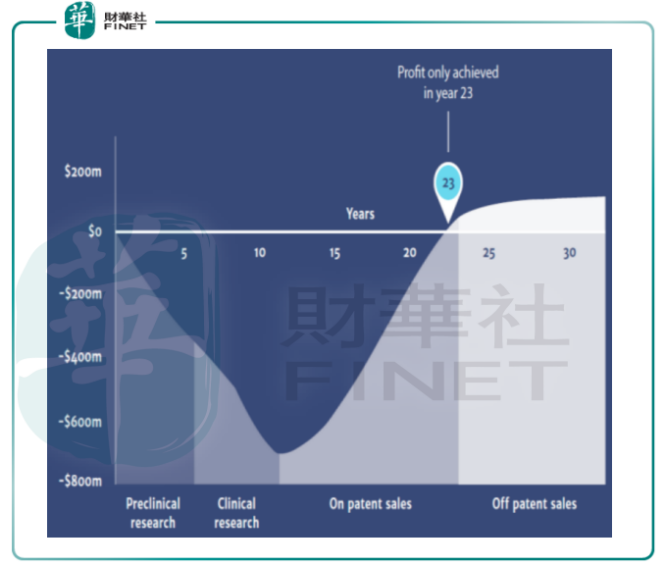
道高一尺,魔高一丈,抗生素的研發必須跟上耐藥菌進化的速度。CDC的綜合數據顯示,從前期培育、中期臨床、後期獲專利上市,抗生素整個產出回報的過程需時23年才能獲得回報:這就意味著如果抗生素研發平台的品種較為單一,就不容易在產品商業化前取得先發優勢。
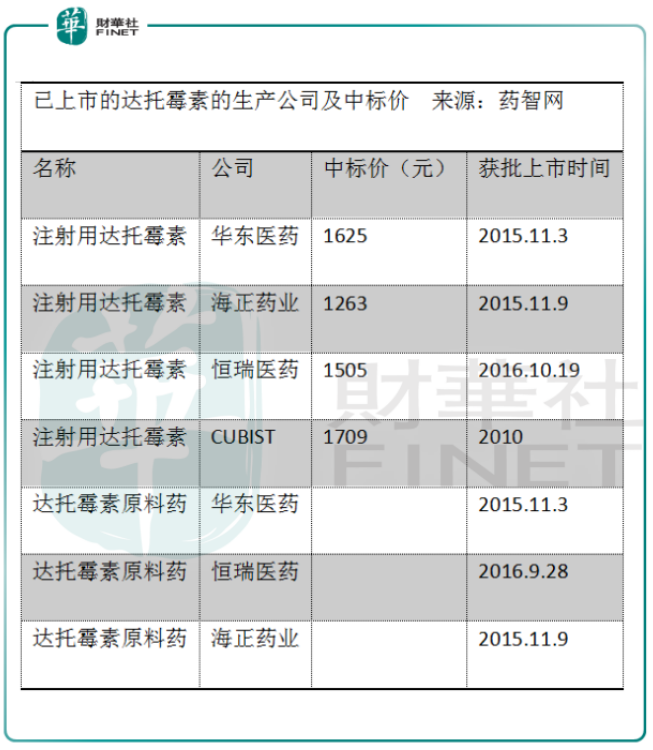
目前市面上生產註射用的達託黴素和達託黴素原料藥這類超級抗菌藥公司不多,國内的隻有海正藥業、恒瑞醫藥、華東醫藥。這三家公司生產的達託黴素製劑的共同點是:都具備註射給藥和口服給藥兩款劑型,且純屬原研藥「克必信」的仿製藥。
「克必信」在2010年於國内成功上市,2014年美聯邦法院宣佈其專利無效,國内達託黴素仿製藥應運而生。2016年,華東醫藥順利通過達託黴素的GMP認證,成為生產達託黴素的國内首家仿製藥公司後,其他藥企亦積極搭建這種超級抗生素的研發平台,除了上述三家藥企外,另還有12家正處於臨床或生產的申請過程中。
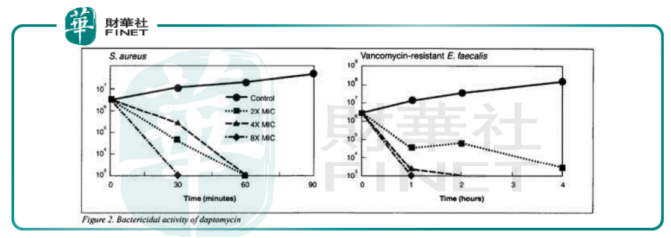
不過與此同時達託黴素殺菌的速度開始放緩,抗生素領域亟需新的重磅藥物登陸,這也成為盟科醫藥最重要的優勢——具備中美同步研發的抗生素突破性產品的多元研發管道。
招股書顯示,盟科醫藥當前共有四條超級抗菌藥的研發管道,分别是Contezolid(MRX-1、MRX-4)、MRX-8(Polymyxin)和MRX-10(LpxC),全部處於臨床試驗階段;其中最可能先上市的Contezolid(MRX-1)是全球首創的對抗多重耐藥革蘭氏陽性菌的口服抗菌藥,可視為達託黴素的「下任接班人」。預期MRX-1最快能在2020年四季度在國内實現商業化,而MRX-1共擁有3項專利,直到2028年才到期。

按照整個研發投入到上市獲利共需時23年這個邏輯來推理,實際上從MRX-1上市直到專利到期再到額外五年非專利營銷專有期,盟科醫藥能否收回它研產抗生素的成本乃至獲利,目前來看還較難預測,而且後面還會有原研抗生素的優勢容易被雨後春筍般起來的仿製藥颠覆的類似劇情。參考達託黴素進入2017年醫保目錄,三大藥企的平均中標價,MRX-1這位超級抗菌藥選手實現商業化之後的命運還有待觀察。
研發難度係數★★★☆☆
抗生素領域的品種,相較於近期的大熱門腫瘤科而言更易被「後來者」居上,一個重要的原因是從臨床試驗共需時長和成功上市的幾率這兩個維度考量,抗生素品種的研發難度屬中等水平。
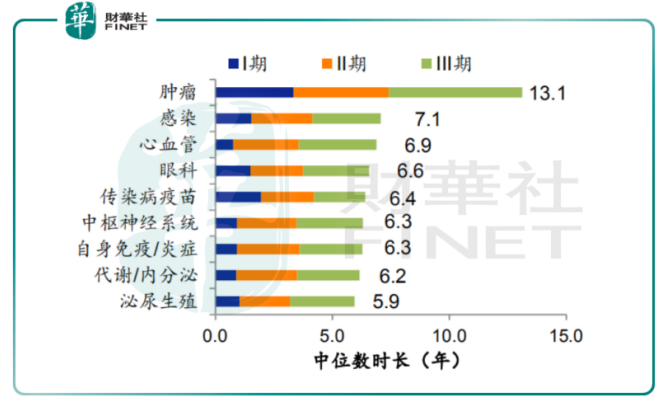
2000年至2017年間,通過對美國的腫瘤、感染、心血管、眼科等9大疾病領域的臨床試驗數據統計,Nature Review Drug Discovery揭露了一款新藥從臨床試驗1期到3期這個過程的平均用時為7.2年;其中腫瘤藥的研發需時13.1年,而抗感染用藥需時低於平均需時,為7.1年,這其中當然會受到美國本土臨床試驗志願者招募的難易程度影響。
從各大疾病領域的藥物成功通過臨床到上市的概率來看,Nature Review Drug Discovery報告顯示,腫瘤領域的用藥順利通過臨床併推出市面的成功率最低,僅為5.1%;血液疾病領域用藥成功率最高,為26.1%;抗感染領域用藥次之,亦高達19.1%;綜合各領域的用藥上市的成功率平均在9.6%左右。
綜合來看,抗感染領域用藥的研發隻要順利渡過臨床2期,基本上就能平安上市。論臨床試驗的進程,目前盟科醫藥已通過臨床2期的隻有MRX-1一款抗生素,另一款治療革蘭氏陽性多重耐藥菌的主力產品MRX-4要等到2019年第一季度才進入臨床1期,而餘下的MRX-8、MRX-10還處於臨床試驗的申請過程中。除MRX-1外,盟科醫藥的管道研發未能順利通過臨床試驗的風險還是較高。
站隊赴港上市之未盈利生物藥研發藥企
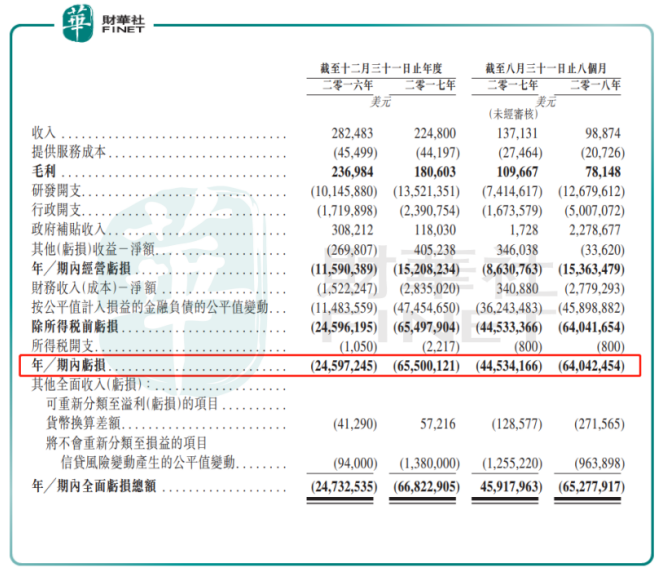
毫無疑問,盟科醫藥又是一位享受新規紅利但尚未盈利的新晉選手。參照同類抗生素的研發上市公司,盟科醫藥的MRX-1和MRX-4與Tetraphase Pharmaceuticals Inc.的四環素類新藥獲批上市前的市場境況類似,而Tetraphase Pharmaceuticals Inc.在該藥獲批時對應市值為5.74億美元(FDA),但中國的超級抗菌藥的原研空白更甚於美國,估計盟科醫藥的參考市值能超過6億美元。
2018年4月港交所上市新規上線以來,吸引了大批尚未盈利或未有收入的生物創新藥獨角獸赴港,而隨著君實生物(01877-HK)、信達生物(01801-HK)的PD-1的獲批上市,國内生物藥市場基本形成跨國藥企(默沙東、羅氏、施貴寶、阿斯利康)和本土藥企(恒瑞醫藥、君實生物、信達生物、百濟神州(06160-HK))對峙的格局。
從領域上看,近期申請赴港上市的生物藥藥企各有細分的方向,比如佈局腫瘤免疫的基石藥業,專註大小分子的靶點研發;繼承母公司綜合管線基因的復宏漢霖,做好生物類似藥爆發的迎接姿勢等,在創新藥談判定價、仿製藥集中採購的醫改下,控費一定會加劇行業的風險,但同時真正有實力的龍頭也將斬獲紅利,而在抗生素這個要長期跟進研發、絕對龍頭尚未坐穩的領域,位處抗生素研發前沿的藥企,尚有市場拓展空間。
財華網所刊載內容之知識產權為財華網及相關權利人專屬所有或持有。未經許可,禁止進行轉載、摘編、複製及建立鏡像等任何使用。
如有意願轉載,請發郵件至 content@finet.com.hk,獲得書面確認及授權後,方可轉載。