今早的消息是從疫情「吹哨人」李文亮醫生於2月7日淩晨因公殉職的死訊中開始的。非常時期,人人都太期待好消息,於是從今早起,各大微信群、自媒體開始瘋傳:
中日友好醫院在武漢疫區牽頭開展瑞德西韋(Remdesivir)治療2019-nCoV新型冠狀病毒臨床研究,為抗擊疫情帶來曙光。
該消息還進一步顯示, 臨床試驗顯示,用藥以後17個小時,病人就恢復了96%的肺功能!到2月4日,所有參加臨床試驗的270名病人的肺部功能都正在恢復!
但問題是,關於瑞德西韋的臨床研究才剛開始2天,怎麽可能知道結果?果不其然,早在臨床研究啓動當天,網上便傳言瑞德西韋短期内在761位患者身上「全部顯效」的說法。
同日,中日友好醫院副院長曹彬教授向媒體表示,瑞德西韋是美國一款處於研發階段的藥物,作用尚有待驗證,也未在任何國家上市。2月5日下午,中日友好醫院王辰、曹彬團隊在武漢市金銀潭醫院宣佈啓動瑞德西韋治療新冠病毒的臨床治療。曹彬教授強調:「臨床研究今天才開始,怎麽可能知道結果?」
由此證實有關瑞德西韋的臨床結果純屬謠言。非常時期,非常心態,所有關於疫情的消息都引人注目、吸足眼球。但互聯網時代,甄别消息的真實性是必修課。
和SARS相比,本次新型冠狀病毒具備致死率較低但傳染性較高的特點,疫情發展整體上也比SARS復雜,這是因為——
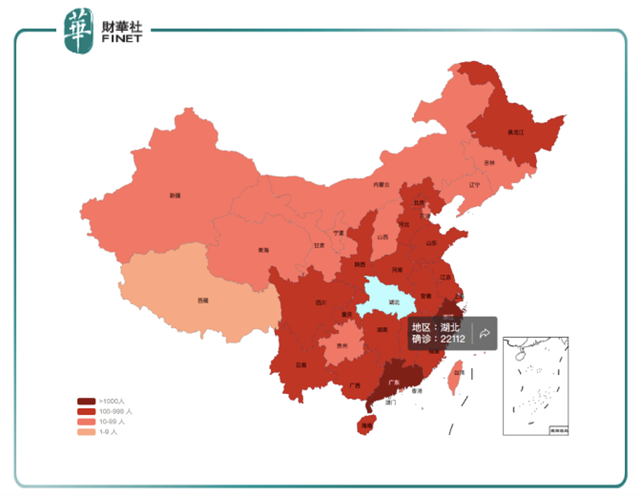
從擴散範圍來看,SARS主要在廣東、北京兩地爆發,2019-nCoV全國爆發,超過200例確診病例的省份、直轄市達到13個2019-nCoV的擴散範圍遠大於SARS;
從感染者數量來看,SARS報告發病數量累計8069人,2019-nCoV目前已經超過2萬人,感染人群遠大於SARS;
從病毒致死率來看,SARS死亡率達到9.59%,而2019-nCoV死亡率在2%左右,非湖北地區死亡率僅有0.2%左右,致死率遠低於SARS。
從發現到基本消除SARS,疫情發展超過7個月,分為發現、蔓延、控制(反復)和解除4個階段,基本上只要控制好「超級傳播者」就能截斷感染途徑,但從上面3個因素,基本可以判斷,2019-nCoV疫情的發展應該更為復雜。
從從衛健委公佈的每日數據來看,全國累計確診病例和累計疑似病例處在持續上升階段(截至2 月7日16:38,兩者數據分别為31,252例、26,359例)。
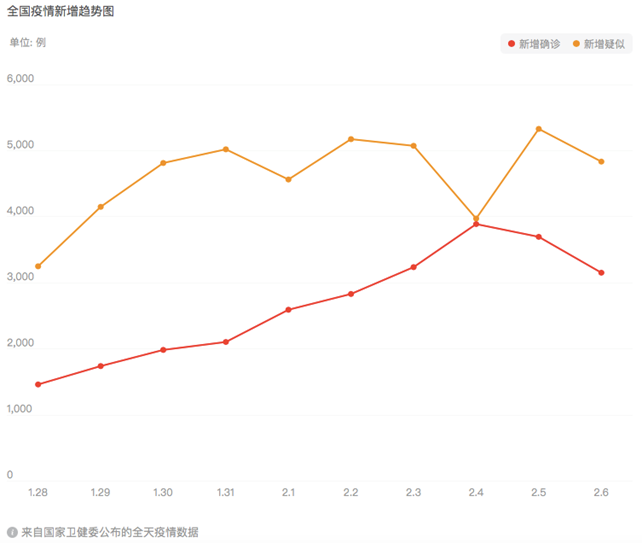
從邊際上來看,新增疑似病例數仍然保持在較高的水平,但已經呈現下降的趨勢。從1 月30 日24:00-2 月3 日24:00,連續5 日新增5,000 例左右;2月4日24:00-2月6日24:00,每日平均新增3,000- 4,000例。考慮到在醫學觀察一段時間之後,部分疑似病例會被排除掉,因此目前來看疫情是開始呈現穩定的趨勢的。
但是從更大範圍的樣本看,全國每日新增醫學觀察數量仍然在持續上升,而且數值龐大(截至2020年2月6日24時,全國累計醫學觀察數量達到18.6萬人,累計追蹤到密切接觸者31.4萬人),而且考慮到統計數據的準確性,現在難言疫情控制的拐點到來。
誠如上文而言,疫情發展具備高度復雜性,有可能出現反復的峰值。根據衛健委專家組判斷,全國確診的第一個峰值可能在1-2週内到來,我們仍需密切觀察疫情是會不會有第二個、第三個峰值。
可喜可賀的是,儘管網傳的瑞德西韋志試驗結果是謠言,但還有一款潛力藥物將可能成為 2019-nCoV的克星,或是這次新冠肺炎的備選解藥——它的名字叫洛匹那韋/利託那韋。
早在2月2日,泰國當地時間2月2日14時,泰國副總理兼衛生部長阿努廷召開新聞發佈會稱,針對新冠病毒,泰國賈維奇醫院(Rajavithi Hospital)的格里昂薩專家團隊發現了一個快速且有效的治療用藥方案。
新冠重症患者使用該方案48小時後情況轉好,檢測新型冠狀病毒核酸結果呈陰性。該治療用藥方案主要包含抗病毒復方製劑洛匹那韋/利託那韋。從本月初開始,洛匹那韋/利託那韋便成為繼瑞德西韋後受高度關注的抗新型冠狀病毒的潛力抗病毒藥物。
經查詢,洛匹那韋/利託那韋是艾滋病二線用藥,它與其它抗反轉錄病毒藥物聯合用藥,來治療成人和2歲以上兒童的人類免疫缺陷病毒-1(HIV-1)感染,及作為一線治療失敗或耐藥的換藥方案。
2000年在美國上市,2004年它應用在SARS治療時並未在國内上市。從藥效機理上講,洛匹那韋/利託那韋是特異性針對HIV的蛋白酶抑製劑,新型冠狀病毒與HIV一樣,都屬於RNA病毒,藥物作用機理一致。
SARS期間,香港大學SARS研究小組的研究者們通過體外藥敏試驗,量化了SARS冠狀病毒對這組抗病毒復合製劑的體外抗病毒活性,並隨後開展了臨床試驗。
研究者們使用洛匹那韋/利託那韋片聯合當時臨床針對非典患者使用的利巴韋林進行對照實驗,發現聯合用藥的41名患者相比常規用利巴韋林的111名患者,死亡率從28.8%降低至2.4%,試驗結果支持洛匹那韋/利託那韋片對SARS患者具有顯著療效。
不過,美國有相關研究報告顯示,經過臨床10餘年的應用實踐表明,洛匹那韋/利託那韋具有的不良反應主要是胃腸道反應、脂肪代謝異常等。但值得注意的是,使用洛匹那韋/利託那韋用於治療HIV耐藥病人的研究樣本量小,存在局限性,因此不能忽略這款潛力備選解藥在治療新冠肺炎病毒的後遺症。
藥物研發之所以要經過臨床一二三期的實驗,是因為治病救命講究數據支撐下的嚴密和嚴謹,這背後體現是對生命的尊重。我們應該認識到,藥物的研發有它的客觀規律,從藥企研發立項到上市需要經歷數年甚至更長的週期。
從海外引進尚未進行臨床一二期的藥物直接在國内進入臨床三期,這是歷史上罕見的現象,而最壞的結果可能是緊急公共衛生事件遠水解不了近渴。
在這場抗疫戰中,針對新冠肺炎的特效藥儘快出現是我們每個人的期盼。2月7日淩晨,武漢中心醫院官方微博發佈消息表示,該院眼科醫生李文亮因感染新型冠狀病毒肺炎,經搶救無效,已於 2月7日淩晨 2點 58 分去世。致此,向李文亮醫生致以沉重的哀悼,也向奮鬥在一線的醫護人員致敬!
財華網所刊載內容之知識產權為財華網及相關權利人專屬所有或持有。未經許可,禁止進行轉載、摘編、複製及建立鏡像等任何使用。
如有意願轉載,請發郵件至 content@finet.com.hk,獲得書面確認及授權後,方可轉載。